Dinosaure, Mammouth, Neandertal... Ils Peuvent Revivre |
Le Génie Génétique au bord de l'Exploit |
 Il y a 20 ans, Jurassic Parc en faisait une réalité virtuelle ; or, voici que la science est au bord d'en faire une réalité biologique ! Trois projets cherchent à ressusciter des espèces disparues. Pas m'importe lesquels : l'un veut faire revivre un dinosaure, l'autre un mammouth et le troisième un homme de Neandertal ! Au-delà des questions qu'ils posent, ces projets font exister un vertige : celui de voir renaître ce qui fut. Pour de vrai.
Il y a 20 ans, Jurassic Parc en faisait une réalité virtuelle ; or, voici que la science est au bord d'en faire une réalité biologique ! Trois projets cherchent à ressusciter des espèces disparues. Pas m'importe lesquels : l'un veut faire revivre un dinosaure, l'autre un mammouth et le troisième un homme de Neandertal ! Au-delà des questions qu'ils posent, ces projets font exister un vertige : celui de voir renaître ce qui fut. Pour de vrai.
Leur pouvoir de fascination, elles le tirent avant tout de leur disparition. Depuis des milliers ou des millions d'années, elles dorment dans les profondeurs de la Terre, réduites à l'état de squelettes emblématiques. Leur mise au jour a engendré des légendes, mais elles-mêmes furent bien réelles : ce sont toutes ces espèces disparues, mineures ou écrasantes, que nous n'arrivons pas à oublier - et que notre imagination se plaît à ressusciter encore et toujours. Parce que, tout de même... et s'il était possible de voir un jour de ses yeux un mammouth, ce mythique mastodonte disparu depuis cinq mille ans ? Ou un dinosaure ? Que ressentirait-on à croiser celui qui domina le monde il y a plusieurs dizaines de millions d'années, avant que ses os ne soient réduits en poudre ou transformés en pierre ? Mais le plus vertigineux serait peut-être de se retrouver face à notre alter ego ; un homme de Neandertal en chair et en os, qui peuplait encore l'Europe il y a trente milliers d'années.
On peut rêver, guère plus... Sauf que trois scientifiques annoncent de tels projets. Le premier, George Church, estime qu'il serait possible de ramener Neandertal à la vie pour 30 millions de dollars. Le second, Akira Iritani, promet de faire naître un mammouth viable d'ici quatre ou cinq ans. Et le dernier, Jack Homer, pense qu'il ne lui faudra pas plus de temps pour donner vie à quelque chose qui ressemblera de près à un dinosaure... Délires d'illuminés ? Certes non : ces trois chercheurs travaillent dans de prestigieuses institutions. George Church, généticien à la Harvard Medical School, à Boston (États-Unis), est l'un des chefs de file de l'ingénierie génétique et de la "biologie synthétique", ce nouveau domaine qui s'attache à explorer des formes de vie artificielle. Akira Iritani, généticien à l'université de Kinki, à Osaka Japon), est l'un des plus éminents biologistes du pays, responsable il y a trente ans de l'une des premières fécondations animales in vitro. Jack Homer, paléontologue à l'université d'Etat du Montana (Etats-Unis), est, lui, l'un des meilleurs spécialistes mondiaux des dinosaures.
Depuis la découverte en 1953 de la structure de la molécule d'ADN, support du patrimoine génétique de tout le vivant, les progrès des biotechnologies ont été tellement fulgurants que même les auteurs de science-fiction ont été dépassés. Pour faire revivre un dinosaure, un mammouth ou un homme de Neandertal, ils envisageaient plutôt de voyager dans le temps afin de ramener à notre époque quelques spécimens des temps révolus ; ou bien ils comptaient sur la chance pour découvrir dans la glace un antique individu parfaitement préservé. Au début des années 1990, le film Jurassic Park (dont Jack Homer fut conseiller scientifique) fut le premier à suggérer une solution qui ne viendrait pas de la physique mais de la biologie : c'est la découverte d'un bloc d'ambre abritant des moustiques gorgés de sang de dinosaures qui permettait, après décryptage et clonage, la recréation des redoutables sauriens. Las, cette technique n'a aucune chance de succès. La structure de l'ADN se dégrade inexorablement avec le temps et devient indécryptable après une centaine de milliers d'années - a fortiori après plusieurs dizaines de millions.
C'est là qu'interviennent nos trois spécialistes. Car, selon eux, il existe différents moyens de ressusciter une espèce disparue. Sachant que tout dépend du matériel biologique disponible - on ne s'attaque pas de la même façon à un dinosaure, à un mammouth ou à un homme de Neandertal. Pour le mammouth, le défi est presque classique : il existe des dépouilles congelées, impressionnantes de fraîcheur apparente. Akira Iritani fait le pari que l'une d'elles contient des cellules en assez bon état pour permettre un clonage, avec pour mère porteuse une éléphante. Une technique qui, depuis le clonage de la brebis Dolly en 1996, a fait ses preuves. Le clonage réussi d'une souris congelée réalisé en 2008 avait ravivé les espoirs. Rendez-vous dans quelques années pour voir ce qu'il en est du parent laineux de l'éléphant. Pour l'homme de Neandertal, la situation est plus compliquée : il n'y a pas de corps conservé permettant d'envisager un clonage. Mais il existe des squelettes assez récents et bien préservés pour que de l'ADN soit extrait des cellules osseuses. C'est ainsi que le séquençage du génome de notre cousin a été réalisé en 2010. Avec ce patron en main, George Church pense possible de transformer la séquence de six milliards de lettres d'un ADN humain en y intégrant les différences constatées entre lui et son cousin, avant d'introduire ce génome modifié dans une cellule idoine. De quoi redonner vie à l'autre grande espèce d'Homo ?
REMONTER LE COURS DE L'ÉVOLUTION
Pour le dinosaure, la situation est encore différente : impossible de récupérer une cellule ou un génome. Jack Homer, avec le généticien Hans Larsson, compte ici suivre une trace plus originale : recréer le mythe à partir d'embryons d'oiseaux, qui en sont les derniers descendants vivants.
Clonage cellulaire, réécriture génétique, reprogrammation embryonnaire : en plongeant dans les trois techniques de résurrection, on comprend l'ampleur et les limites de la révolution biotechnologique. Et ces projets ne manquent pas de poser des questions éthiques ou écologiques. Mais ils prouvent que le génie génétique maîtrise de mieux en mieux la vie à toutes ses échelles. Au point de faire renaître ce qui n'est plus ?
E.R avec L.B. - SCIENCE & VIE > Décembre > 2011 |
|
Faire Revivre des Dinosaures... par la Manipulation d'Embryon |
Quand Jurassic Park a débarqué sur les écrans en 1993, ce fut l'émoi. Jamais dinosaure n'avait paru si réel ! Mais ce n'était pas encore assez pour Jack Homer, qui fut conseiller scientifique du film de Spielberg, garant de ce réalisme.
Car ce qu'a toujours voulu ce spécialiste mondialement reconnu des dinosaures, c'est pouvoir en toucher un, en vrai. Le problème, s'il fallait n'en citer qu'un, est que les dinosaures ont disparu il y a quelque 65 millions d'années. D'eux, il ne reste que des squelettes de pierre, désertés depuis bien longtemps de toute vie et de toute trace d'ADN, qui renferme le patrimoine génétique.
Jack Homer le sait bien, mais n'y voit pas un problème. "Pas besoin d'ADN ancien, note-t-il tranquillement. Les oiseaux sont les descendants des dinosaures : ils portent cet ADN ancestral ! La majeure partie du programme génétique concernant les traits des dinosaures que nous voulons ressusciter est toujours là, chez les oiseaux - chez le poulet, par exemple. "D'où une idée aussi simple qu'originale : "Réveiller le dinosaure qui sommeille en chaque poulet". En gros, partir de la volaille pour lui faire parcourir en sens inverse le chemin que l'évolution lui a fait prendre depuis quelques  dizaines de millions d'années, et faire réapparaître ces traits ancestraux perdus au fil du temps.
dizaines de millions d'années, et faire réapparaître ces traits ancestraux perdus au fil du temps.
Quels traits ? En comparant les ossatures du T. rex et de son très lointain petit-neveu, le paléontologue s'est concentré sur les différences les plus emblématiques - à savoir la perte de la queue, des mains griffues et du museau dentu. Qu'on les fasse revenir, et on obtiendra quelque chose qui ressemblera beaucoup plus à un petit raptor qu'à un banal gallinacé. Voilà la ligne directrice qu'il a tracée pour faire d'un poulet un néodinosaure, un "pouletosaure", comme il l'appelle.
Le point de départ de ce vaste projet est l'embryon. En effet, "lors d'un stade précoce de son développement embryonnaire, le poulet possède des traits dinosauriens comme une longue queue (->), des dents et des mains à trois doigts, souligne le professeur. Des traits qui disparaissent ensuite, comme les ébauches de branchies de notre propre vie embryonnaire. Si vous trouvez les gènes qui causent la disparition de la queue ou provoquent la fusion des doigts pour constituer une aile, et que vous éteignez ces gènes, vous verrez grandir un animal qui possède certaines des caractéristiques des dinosaures".
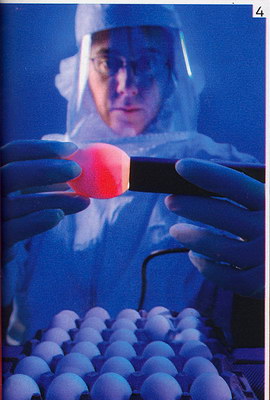
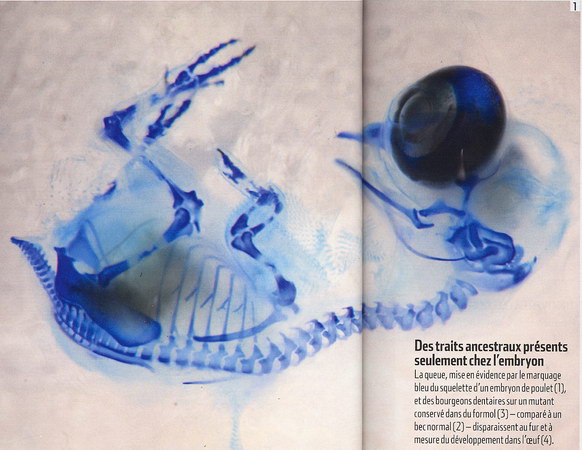
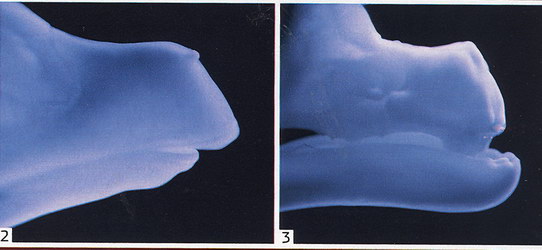 Serait-ce donc aussi simple ? En tout cas, en 2006, une étude de Matthew Harris et John Fallon a prouvé que ce type d'expérimentation n'était pas une douce utopie. Alors qu'il étudiait des embryons de poulets mutants, Matthew Harris en découvrit un spécimen conservé dans du formol dont le bec semblait garni de... bourgeons dentaires ! Un poulet qui aurait des dents ? L'idée fait sourire, elle remonte pourtant à ses origines sauriennes. Pour en avoir le cour net, le chercheur entreprit de stimuler, par ajout de facteur de croissance, la production d'une protéine précise chez un embryon normal pour voir s'il pouvait reproduire ce curieux constat. Et ce fut le cas !
Serait-ce donc aussi simple ? En tout cas, en 2006, une étude de Matthew Harris et John Fallon a prouvé que ce type d'expérimentation n'était pas une douce utopie. Alors qu'il étudiait des embryons de poulets mutants, Matthew Harris en découvrit un spécimen conservé dans du formol dont le bec semblait garni de... bourgeons dentaires ! Un poulet qui aurait des dents ? L'idée fait sourire, elle remonte pourtant à ses origines sauriennes. Pour en avoir le cour net, le chercheur entreprit de stimuler, par ajout de facteur de croissance, la production d'une protéine précise chez un embryon normal pour voir s'il pouvait reproduire ce curieux constat. Et ce fut le cas !
AJOUT DE PROTÉINES DE CROISSANCE
"Par une simple manipulation, l'ajout de protéines et de facteurs de croissance, des dents rudimentaires rappelant celle des alligators ont poussé chez l'embryon de poulet et sa mâchoire s'est modifiée, se rappelle ce biologiste du département de génétique d'Harvard. Notre travail a beaucoup intrigué parce qu'il montre qu'il est possible de réactiver des capacités et des structures considérées comme perdues. "Une publication fondatrice, aujourd'hui au cour d'un travail en cours dans le laboratoire du professeur Arkhat Abzhanov, de Harvard. Son objectif : comprendre les mécanismes en jeu derrière ces altérations du bloc dents-mâchoires et les signaux moléculaires qui les dirigent - pour en prendre le contrôle. Tout comme Homer, qui se focalise lui sur la queue et les membres supérieurs.
Pour mettre les mains dans ce cambouis moléculaire, le paléontologue s'est tourné vers le généticien Hans Larsson, de l'université McGill (Canada). Ce spécialiste de "l'atavisme expérimental" cherchait déjà à pousser des animaux actuels à réexprimer des traits ancestraux. Depuis 2008, son équipe travaille à suivre les réseaux d'activation de gènes chez l'embryon de poulet, analysant les réactions biochimiques et génétiques à l'ajout de cocktails de protéines de contrôle et de facteurs de croissance.  Le but : identifier quand, comment et où agir dans l'embryon pour voir se maintenir chez lui les traits sauriens tant désirés (infographie ->). Les deux passionnés ont déjà obtenu quelques résultats et Jack Homer a donné rendez-vous dans cinq ans... Tous les spécialistes ne sont toutefois pas convaincus de la faisabilité de la chose.
Le but : identifier quand, comment et où agir dans l'embryon pour voir se maintenir chez lui les traits sauriens tant désirés (infographie ->). Les deux passionnés ont déjà obtenu quelques résultats et Jack Homer a donné rendez-vous dans cinq ans... Tous les spécialistes ne sont toutefois pas convaincus de la faisabilité de la chose.
DES INFORMATIONS MANQUANTES
"Quoique passionnant intellectuellement, ce projet a des points faibles, tempère Matthew Harris. Beaucoup de choses peuvent être retrouvées dans l'ADN, mais il y a des pertes d'information : par exemple, on ne retrouve pas le gène de l'émail dentaire chez le poulet. Et on ne sait pas comment se déroulait le développement embryonnaire d'un dinosaure, quels gènes opéraient et comment ils interagissaient". Jack Homer et Hans Larsson ont conscience de cette complexité. Ils ont aussi toujours pris garde de ne pas prétendre que leur pouletosaure serait un T rex, ou un autre des reptiles mythiques. Ils ont également prévu qu'au moindre signe que leur "bébé" ne pourrait pas vivre dans de bonnes conditions, ils ne le laisseront pas éclore ; sachant qu'il n'y a ici "aucun danger de propagation : c'est le développement du poulet qui est altéré, non son génome. S'il se sauvait ou copulait (ce qui n'est pas prévu), le résultat serait un poulet normal". Et il ne s'agit pas non plus de lancer une production à grande échelle. Il y aurait donc, dans le meilleur des cas, un unique pouletosaure, membre unique d'une espèce virtuelle - mais en soi, cette possibilité vaudrait tous les films de fiction...
 À LA RECHERCHE D'AUTRES CANDIDATS... À LA RECHERCHE D'AUTRES CANDIDATS...
Recréer un animal disparu en transformant un de ses cousins vivants…
L'idée bluffe, mais elle est difficile à mettre en ouvre. "Il faut un descendant actuel et un animal modèle sur lequel mener des travaux de génétique notamment, pose François Bonneton, généticien et évolutionniste à l'université de Lyon. Il faut aussi de bonnes données paléontologiques pour connaître l'état ancestral d'une espèce". Or, mis à part les dinosaures, trouver le candidat idéal n'est pas évident... Mouche et scarabée ont déjà été ramenés à un stade antérieur. Mais pour des espèces plus attendues, ici le dodo, il manque des éléments : un cousin proche, le pigeon, a été identifié, mais il n'est pas son ancêtre. |
E.R avec L.B. - SCIENCE & VIE > Décembre > 2011 |
|
Faire Revivre un Mammouth... par le Clonage Cellulaire |
Vingt ans qu'il y pense. Il a même déjà tenté trois fois en quinze ans la délicate manipulation - sans succès... Mais aujourd'hui, avec les avancées de la biologie moléculaire, Akira Iritani, de l'université de Kinki, au Japon, a le sentiment qu'il va enfin pouvoir mener à bien son ambitieux projet : cloner un mammouth.
Et si la technique commence à se banaliser pour certaines espèces très étudiées, l'expérience prend ici un caractère tout à fait exceptiçmnel. Rien de rédhibitoire pour le généticien nippon, pour qui faire revivre le proboscidien laineux tient autant du devoir que de la recherche scientifique.
Le clonage ? Popularisée depuis 1996 par la brebis Dolly, cette technique consiste à injecter le noyau (et son précieux ADN) d'une cellule appartenant à un individu "A" dans un ovule "B" dont on a au préalable ôté le noyau ; la cellule obtenue est ensuite stimulée électriquement et implantée dans l'utérus d'une mère porteuse. Si B apporte certains éléments lors du développement embryonnaire, tout comme la mère porteuse, c'est cependant A qui est cloné. Habituellement, donneur, ovocyte et mère porteuse sont vivants et de la même espèce (avec des taux de réussite variables : il fallut 277 oufs fécondés pour obtenir Dolly) ; pour le mammouth, la situation sera indéniablement moins classique...

 Concernant le problème très matériel mais incontournable de l'ovule et de la mère porteuse réquisitionnée, le mammouth ayant depuis longtemps disparu, il faut se résoudre à se tourner vers une autre espèce. En l'occurrence, l'éléphant d'Afrique, son plus proche parent. Toutefois, les éléphantes ne produisent qu'un unique ovule tous les quatre mois environ et, pour peu qu'elles deviennent gestantes, cinq ans d'attente sont nécessaires avant qu'elles ne relancent un cycle de maturation de ces précieuses cellules reproductrices. La solution ? L'équipe d'Akira Iritani a contacté les zoos du Japon pour qu'ils leur cèdent les ovocytes à la mort de leurs éléphantes. Pas besoin donc de prélèvements compliqués et risqués pour ces dernières.
Concernant le problème très matériel mais incontournable de l'ovule et de la mère porteuse réquisitionnée, le mammouth ayant depuis longtemps disparu, il faut se résoudre à se tourner vers une autre espèce. En l'occurrence, l'éléphant d'Afrique, son plus proche parent. Toutefois, les éléphantes ne produisent qu'un unique ovule tous les quatre mois environ et, pour peu qu'elles deviennent gestantes, cinq ans d'attente sont nécessaires avant qu'elles ne relancent un cycle de maturation de ces précieuses cellules reproductrices. La solution ? L'équipe d'Akira Iritani a contacté les zoos du Japon pour qu'ils leur cèdent les ovocytes à la mort de leurs éléphantes. Pas besoin donc de prélèvements compliqués et risqués pour ces dernières.
Reste le donneur, c'est-à-dire le mammouth. Lui est mort et congelé depuis quelques milliers d'années. En conséquence, son noyau cellulaire est forcément dénaturé et son ADN en lambeaux - dès que survient la mort, diverses réactions chimiques s'y attaquent. Trouver une cellule suffisamment préservée pour permettre le clonage n'est donc pas évident. Les merveilleuses momies de bébés mammouths récemment exhumées du permafrost sibérien peuvent laisser croire que ce souci est écarté... Trompeuse illusion ! Le froid qui a protégé leur apparence n'a pas épargné leurs cellules : la congélation n'est pas assez rapide pour empêcher toute dégradation, et les cristaux de glace qui se forment les déchirent de l'intérieur. Oui, mais en 2008, Teruhiko Wakayama, un autre généticien japonais, réussissait à cloner une souris restée seize ans dans un congélateur. Un espoir pour Akira Iritani qui, dès 2009, s'est inspiré des travaux de son collègue pour tenter de cloner un animal congelé autrement plus imposant : un taureau. Et ce fut une réussite !
TROUVER LA CELLULE ADÉQUATE
Parallèlement, son équipe se lançait dans la récupération de l'ADN nucléaire d'un mammouth pour tester son injection dans des ovules de souris. "Nous avons démontré que la récupération du noyau d'une cellule morte depuis une longue période était possible, de même que sa transplantation dans un ovocyte. Ceci est le premier pas vers la résurrection d'animaux anciens", concluait sa publication scientifique. Un premier pas toutefois incomplet puisque cet ADN resta muet... D'autres pas restaient donc à franchir. Le premier d'entre eux étant d'obtenir une cellule de mammouth en parfait état, condition sine qua none pour tenter de récupérer son noyau, comme Akira Iritani l'annonçait courant 2011 : "Les problèmes techniques ont été résolus et les opérations préparatoires devant nous permettre d'atteindre notre but ont été menées. Tout ce dont nous avons besoin maintenant, c'est d'un bon échantillon de tissu prélevé sur un mammouth encore gelé. "Pour ce faire, le professeur prévoyait cet été une expédition en Sibérie, dont la terre gelée a été jusqu'ici la meilleure pourvoyeuse en momies glacées de mammouths. Pour l'heure, ses résultats ne sont pas connus mais, en cas d'échec, des accords avec des laboratoires russes devraient lui donner accès à des carcasses déjà exhumées et bien préservées. De quoi tester les cellules de différents tissus pour sélectionner les plus belles, et lancer la manipulation avec ces heureuses élues... 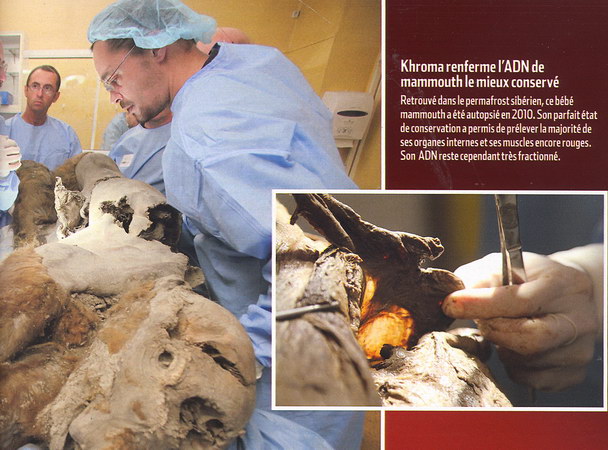 Sauf que les spécialistes de l'ADN ancien sont unanimes : "J'ai eu la chance de travailler sur de nombreux tissus de mammouth, intestin, foie, reins... mais aussi poils ou os pour en extraire l'ADN. Et, à chaque fois, l'ADN est en kit"... pointe Régis Debruyne, du Muséum national d'histoire naturelle de Paris, associé au programme de recherche spécialisé "Mammuthus". Le jeune paléogénéticien a pourtant eu accès aux plus beaux spécimens récemment dégagés, tels les bébés Lyuba et Khroma : "Le génome du mammouth fait quatre milliards et demi de paires de bases, contre trois chez l'homme. Chez Khroma, qui est le mieux conservé, nous sommes ravis quand on récupère des fragments de 2000 paires de bases !"
Sauf que les spécialistes de l'ADN ancien sont unanimes : "J'ai eu la chance de travailler sur de nombreux tissus de mammouth, intestin, foie, reins... mais aussi poils ou os pour en extraire l'ADN. Et, à chaque fois, l'ADN est en kit"... pointe Régis Debruyne, du Muséum national d'histoire naturelle de Paris, associé au programme de recherche spécialisé "Mammuthus". Le jeune paléogénéticien a pourtant eu accès aux plus beaux spécimens récemment dégagés, tels les bébés Lyuba et Khroma : "Le génome du mammouth fait quatre milliards et demi de paires de bases, contre trois chez l'homme. Chez Khroma, qui est le mieux conservé, nous sommes ravis quand on récupère des fragments de 2000 paires de bases !"
UNE SOLUTION SYTNTHÉTIQUE
Même constat chez Stéphane Schuster, qui a dirigé le séquençage du génome du mammouth en 2008 : "L'ADN est trop fracturé pour que l'on puisse travailler avec. Sans parler des chromosomes qui sont évidemment perdus". Parvenir à lire l'ADN a ainsi tenu de la gageure avec un résultat final complet à 80 %, mais difficilement exploitable tant il est fractionné. Au final, il n'est donc pas sûr que le professeur Iritani puisse trouver sa cellule au noyau et au génome quasiment intacts.
Mais tout n'est pas perdu. Certains spécialistes suggèrent en effet une autre option : plutôt que de chercher une hypothétique cellule idéale, pourquoi ne pas la créer ? La séquence de l'ADN du mammouth étant désormais largement connue, il "suffirait" de reconstituer les chromosomes (en s'inspirant de ceux d'un éléphant, qui en possède 56) et un noyau artificiel pour les y placer. Or, certaines technologies d'ingénierie génétique et de biologie moléculaire commencent déjà à obtenir des premiers résultats sur des cellules rudimentaires.
Evidemment, on est encore loin d'une cellule artificielle de mammouth, mais c'est une piste. Qui pourrait conduire au dernier problème se trouvant sur la route de la résurrection du grand disparu : trouver un moyen d'implanter chez une éléphante d'Afrique l'embryon né dans les labos. Son utérus est en effet situé à 2,5 m de profondeur ! Une performance jamais tentée. Qu'elle réussisse, et on aura la réponse à la question que tout le monde se pose : quelle sorte de mammouth naîtrait effectivement de tant d'efforts ?
 À LA RECHERCHE D'AUTRES CANDIDATS... À LA RECHERCHE D'AUTRES CANDIDATS...
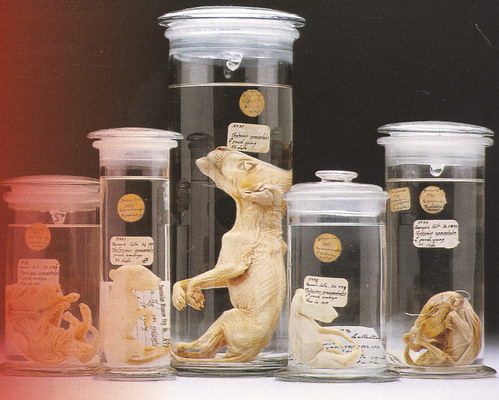
Quel reste biologique d'animal disparu pourrait être en assez bon état pour permettre un clonage ?
Plusieurs phénomènes chimiques et des environnements plus ou moins naturels momifient le corps : le permafrost, les tourbières, certaines cavernes ou des déserts secs ; le formol est aussi utilisé pour conserver artificiellement les tissus. On dispose ainsi d'animaux anciens incroyablement préservés - comme le tigre de Tasmanie, disparu depuis 1936. Mais le constat est généralement le même : si l'apparence est sauve, les cellules sont altérées et l'ADN se retrouve en confettis. Il faut une congélation rapide et intense, par exemple avec de l'azote liquide, pour récupérer des cellules utilisables pour un clonage. |
E.R avec L.B. - SCIENCE & VIE > Décembre > 2011 |
|
Faire Revivre un Homme de Neandertal... par la technique de Réécriture Génétique |
George Church est le roi de la formule choc - mais c'est aussi un généticien de génie et un jusqu'au-boutiste. Si bien que lorsqu'il déclara en 2009 que l'homme de Neandertal pourrait être ramené à la vie pour 30 millions de dollars, ses collègues ne le prirent pas à la légère.
Deux ans plus tard, ce défi n'a pas été officiellement lancé, essentiellement pour des raisons éthiques. Car sur le plan technique, certains pensent que le jour n'est plus si loin où notre cousin pourrait se dresser devant nous. Grâce aux avancées des biotechnologies, dues pour beaucoup à George Church, et aux connaissances toujours plus approfondies sur les génomes anciens.
Ici, pas de cellules congelées susceptibles d'être exploitées, juste des squelettes en assez bon état et assez récents pour avoir permis, en 2010, à l'équipe de Svante Paabo, du Max Planck Institute (Allemagne), de séquencer à près de 70 % l'ADN de Neandertal, après quatre ans de travail ! Une prouesse inconcevable il y a encore dix ans, et qui a apporté son lot de révélations. À commencer par la proximité entre nos espèces (plus de 99,7 % d'identité entre nos deux patrimoines) et les échanges d'ADN qui nous lient. Mais surtout, cette séquence, le texte brut du génome néandertalien, a offert un matériau de premier choix au généticien de Harvard. Voilà une sorte de clef qui, à peine modifiée, pourrait ouvrir la voie à une autre humanité...

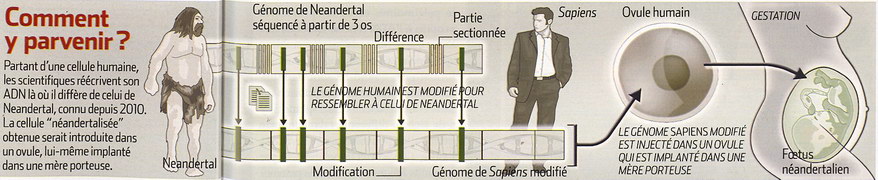 Pour Church, inutile de fabriquer l'interminable molécule d'ADN d'Homo neanderthalensis à partir de zéro. Comme chez Sapiens, elle est composée de plus de trois milliards de paires de bases, ou lettres. Il "suffirait" de prendre une molécule d'ADN d'Homo sapiens, laquelle est séquencée depuis dix ans, et de la retoucher en y intégrant les millions de différences de lettres existant entre notre texte génétique et celui de notre cousin. Deux façons de faire sont ici envisageables, en partant de la molécule de Sapiens et en la modifiant pour l'amener à ressembler à sa contrepartie néandertalienne. La première serait de prendre l'ADN sapiens pour, dans un premier temps, le couper en quelques dizaines de milliers de fragments afin de pouvoir les insérer dans des bactéries : ces précieuses petites usines cellulaires, très utilisées en biotechnologie, ne pouvant prendre en charge de trop longues molécules en raison de leur très petite taille. Ce sont elles qui vont introduire des mutations dans les fragments d'ADN sapiens pour les transformer en leur version néandertalienne. Tous ces fragments modifiés seraient ensuite récupérés, vérifiés et réassemblés en un ADN imitant au plus près celui de Neandertal... y parvenir serait une énorme performance pour les biotechnologies ! Toutefois, même si les techniques actuelles, après des améliorations de rendement, autorisaient une telle réécriture génétique, des spécialistes pointent que la séquence d'ADN brute ne fait pas tout. Il suffit de se rappeler l'image bien connue de nos chromosomes pour s'en convaincre : pour les former, notre long filament d'ADN se replie encore et encore sur lui-même afin de pouvoir d'une part tenir dans nos cellules et, d'autre part, être utilisé de la bonne façon par lesdites cellules. Car ce repliement, assuré par la machinerie cellulaire propre à chaque espèce, est hautement stratégique : il permet de cacher les portions de l'ADN qui ne doivent pas servir et de mettre en avant les autres.
Pour Church, inutile de fabriquer l'interminable molécule d'ADN d'Homo neanderthalensis à partir de zéro. Comme chez Sapiens, elle est composée de plus de trois milliards de paires de bases, ou lettres. Il "suffirait" de prendre une molécule d'ADN d'Homo sapiens, laquelle est séquencée depuis dix ans, et de la retoucher en y intégrant les millions de différences de lettres existant entre notre texte génétique et celui de notre cousin. Deux façons de faire sont ici envisageables, en partant de la molécule de Sapiens et en la modifiant pour l'amener à ressembler à sa contrepartie néandertalienne. La première serait de prendre l'ADN sapiens pour, dans un premier temps, le couper en quelques dizaines de milliers de fragments afin de pouvoir les insérer dans des bactéries : ces précieuses petites usines cellulaires, très utilisées en biotechnologie, ne pouvant prendre en charge de trop longues molécules en raison de leur très petite taille. Ce sont elles qui vont introduire des mutations dans les fragments d'ADN sapiens pour les transformer en leur version néandertalienne. Tous ces fragments modifiés seraient ensuite récupérés, vérifiés et réassemblés en un ADN imitant au plus près celui de Neandertal... y parvenir serait une énorme performance pour les biotechnologies ! Toutefois, même si les techniques actuelles, après des améliorations de rendement, autorisaient une telle réécriture génétique, des spécialistes pointent que la séquence d'ADN brute ne fait pas tout. Il suffit de se rappeler l'image bien connue de nos chromosomes pour s'en convaincre : pour les former, notre long filament d'ADN se replie encore et encore sur lui-même afin de pouvoir d'une part tenir dans nos cellules et, d'autre part, être utilisé de la bonne façon par lesdites cellules. Car ce repliement, assuré par la machinerie cellulaire propre à chaque espèce, est hautement stratégique : il permet de cacher les portions de l'ADN qui ne doivent pas servir et de mettre en avant les autres.
NOS DIFFÉRENCES SYNTHÉTISÉES
La cellule joue également un rôle incontournable dans la bonne régulation de l'expression de la molécule patrimoniale. Or, une séquence brute reconstituée quasi ex nihilo n'aurait accès à aucune de ces informations fondamentales ; un peu comme si nous nous retrouvions avec un guide d'utilisation regroupant sans ordre tous les appareils électroménagers possibles d'une maison, sans schéma ni ponctuation ou chapitre. De là une seconde approche, qui permettrait de pallier une partie de ces problèmes.
Elle s'appuie sur les technologies "Mage" (pour Multiplex automated genome engineering) développées là encore par les laboratoires de George Church. Le principe : modifier in vivo le génome d'une cellule vivante de Sapiens ! Cette fois, il faudrait créer de tout petits bouts d'ADN néandertalien centrés chacun sur une ou plusieurs des différences répertoriées entre notre génome et celui de notre cousin disparu ; les "synthétiseurs d'ADN" actuels font cela couramment. Ces petits bouts seraient ensuite introduits dans ladite cellule dont on veut modifier le patrimoine : certaines propriétés propres à l'ADN font en effet que des bouts qui se ressemblent s'assemblent spontanément et mélangent leurs informations ; quand ils sont parfaitement identiques, c'est évidemment sans conséquence - mais quand il y a de légères différences dans le texte porté, elles peuvent passer de l'un à l'autre. Les "corrections" portées par les petits fragments artificiels peuvent ainsi se retrouver intégrée dans la molécule mère présente dans la cellule.
Aujourd'hui, cette technologie est utilisée en biologie moléculaire chez la mouche ou la souris pour introduire jusqu'à quelques centaines de modifications. Pour effectuer la conversion Neandertall Sapiens, il faudrait être capable de passer à l'échelle du million !
UN EMBRYON DE NEANDERTAL ?
La cellule pourrait alors être utilisée pour créer un embryon, qui serait lui-même implanté dans une mère porteuse. Mais certains doutes subsistent : "Faire le saut, j'ai le génome, je peux recréer l'espèce est un raccourci simpliste, souligne François Bonneton, de l'université de Lyon. On peut bien sûr comparer deux génomes, mais ça reste un travail presque abstrait. Car le génome n'est qu'une molécule - certes, une molécule du vivant, mais il n'est pas vivant lui-même : pour que l'information qu'il porte soit bien lue, il faut la bonne cellule... Et, en l'occurrence, les cellules anciennes dont on aurait besoin n'existent plus". En effet, si la majeure partie des différences de séquences entre Sapiens et Neandertal peut être "corrigée", la cellule, elle, restera fondamentalement sapiens ; elle interagira donc "sapiensement" avec son ADN "neandertalisé". Qui sait alors ce que pourrait donner un tel mélange ? "Un hybride, ni tout à fait l'un ni tout à fait l'autre", pense l'évolutionniste moléculaire français.
George Church, lui, estime que, les premières étapes de développement embryonnaire passées, les gènes néandertaliens pourraient bien prendre le dessus sur leur environnement sapiens. Il est fort à parier qu'un laboratoire ou un autre tentera cette expérience dans les armées à venir - sur le sulfureux couple Sapiens-Neandertal ou sur d'autres moins ambigus. Quel vocable alors utiliser pour le futur individu ? Car il sera difficile de juger de sa "néandertalité" lors du développement de l'embryon... Church admet que, son environnement et sa culture ayant disparu, il serait plus logique de parler de "néo-Neandertal". Mais ces deux composantes essentielles de l'identité, des individus comme des espèces, ne sont pas du ressort de la biologie ni des biotechnologies, qui auront fait leur part du travail.
 À LA RECHERCHE D'AUTRES CANDIDATS... À LA RECHERCHE D'AUTRES CANDIDATS...
Les paléogénéticiens parviennent de plus en plus fréquemment à exhumer des séquences d'ADN ancien d'ossements millénaires conservés dans des conditions adéquates, et même à le faire s'exprimer dans d'autres génomes.
Mais réussir à obtenir le génome entier est une autre paire de manches. Le mammouth et Neandertal sont pour l'heure les seuls à avoir vu leur génome entièrement séquencer... Ce qui ne veut pas dire qu'ils sont condamnés à le rester : le rhinocéros laineux (photo), fréquemment retrouvé dans les sols gelés de Sibérie aux côtés du célèbre mastodonte, semble un parfait candidat. Ours des cavernes et tigre à dents de sabre ont aussi fait l'objet d'études génétiques (pour répondre à des questions d'ordre généalogique, par exemple), mais leur ADN n'est pas reconstitué de bout en bout. |
E.R avec L.B. - SCIENCE & VIE > Décembre > 2011 |
|
Un Moyen de Préserver la Biodiversité ? |
Ressusciter des espèces disparues... Pourquoi faire ? Des zoos ? Un remède à la crise de la biodiversité ? Pas si simple...
D'étranges cris résonnent dans l'immense animalerie. Vous entrez. À gauche, une première division annonce : "Disparus modernes". Deux tigres de Tasmanie y côtoient un dodo et une autruche géante. Un peu plus loin, voici la division des "disparus du cénozoïque", où l'on peut admirer des mammouths, un tigre à dents de sabre, un rhinocéros laineux... Mais ce qui attire le plus de monde, c'est la division du fond : celle des "disparus du mésozoïque", avec des oiseaux-dinosaures au museau dentu, aux griffes acérées et aux ailes pointues qui s'agitent dans une gigantesque volière.
Cette scène, Steven Spielberg l'avait imaginée... et les biologistes moléculaires sont peut-être en train d'en faire une réalité, ouvrant dès lors la voie à de "vrais Jurassic parks". Mais encore ? Redonner vie au passé ne servirait-il qu'à créer de lucratifs parcs à dinosaures ? Cela serait déjà un spectaculaire résultat, certes, mais certains biologistes voient plus loin : la perspective de faire revivre le passé serait surtout l'occasion d'enrayer la crise actuelle de la biodiversité. Effet d'annonce ? Réalité ?
Une chose est sûre : Noé a du souci à se faire. Exit son arche où accueillir toutes les créatures terrestres ; désormais, un petit bout de chaque espèce suffit pour les sauver. Et pas seulement sauver celles en voie d'extinction, mais aussi ressusciter celles déjà disparues ! D'où la multiplication de banques de tissus d'espèces en danger dans l'espoir, un jour, d'aider ces populations à se reconstituer. Pour le biologiste mexicain Raul Pina-Aguilar, "ces pistes biotechnologiques ne représentent pas une solution à tous les problèmes de conservation mais elles pourront, dans certains cas, s'avérer très utiles". Notamment pour les espèces sur le point de disparaître, comme le rhinocéros blanc du Nord.
"Ces espèces sont de toute façon condamnées à s'éteindre. C'est de l'acharnement thérapeutique", conteste Robert Barbault, écologue au Muséum d'histoire naturelle de Paris. Un acharnement qui présenterait au moins l'avantage d'ajouter, pour le clonage, d'autres spécimens aux quelques survivants ; il deviendrait ainsi possible de réintroduire de la diversité génétique dans ces populations en déliquescence. Or, cela offre plus de chances de combinaisons gagnantes face à la prochaine épidémie ou à tout autres modifications de l'environnement, et donc, in fine, une meilleure chance de survie du groupe. Mais qu'en est-il des espèces déjà disparues ? Pourra-t-on, grâce à ces nouvelles prouesses biotechnologiques, envisager de les réintroduire en milieu sauvage ? La tentative la plus aboutie en la matière concerne une sous-espèce de bouquetin des Pyrénées, Capra Pyrenaica, dont le dernier individu est mort en 2000. Neuf ans plus tard, une équipe franco-espagnole est parvenue à lui redonner vie grâce au clonage. Las, ce petit revenant est mort sept minutes après sa naissance : comme la plupart des clones, il souffrait d'une malformation pulmonaire.
MAIS CE MONDE N'EST PLUS LE LEUR !
Admettons cependant que les généticiens parviennent à mieux maîtriser ces techniques : ces espèces ressuscitées pourraient-elles alors s'adapter à leur environnement présent ? Rien n'est moins sûr... Car de deux choses l'une : soit l'espèce a disparu depuis très peu de temps et les raisons environnementales ayant présidé à son déclin sont toujours là ; soit l'espèce a disparu depuis si longtemps que l'environnement qui lui était favorable n'existe plus. Dans les deux cas, peu de chance qu'elle survive durablement dans la nature.
"Pour aider une espèce à se reconstituer, il faut d'abord remettre en fonctionnement son écosystème. C'est un principe de base en conservation" affirme Pierre-Henri Gouyon, spécialiste des sciences de l'évolution au Muséum national d'histoire naturelle de Paris. Certes, certains projets envisagent de reconstruire les écosystèmes du passé, comme en Sibérie, aux Pays-Bas ou en Lituanie, où de grands herbivores (bisons, élans, chevaux) et prédateurs (loups, ours, lynx) sont réintroduits sur de vastes étendues inhabitées, afin de retrouver les paysages de grandes steppes à mammouths de l'époque du pléistocène. Toutefois, ces projets restent très localisés. Et, en dehors de ces zones, les réintroductions risquent de se heurter à des écosystèmes perturbés par les activités humaines. Ainsi, l'homme aura beau s'évertuer à recréer des tigres de Tasmanie, si leur chasse reste pratiquée, l'espèce ne se reconstituera pas.
Ces revenants d'outre-tombe seront-ils acceptés par les populations ? Le simple retour dans nos montagnes d'espèces sauvages existantes comme le loup ou l'ours soulève déjà énormément d'opposition... De surcroît, ces bêtes ne setaient pas la copie conforme de l'espèce disparue puisqu'elles auront été portées par une autre espèce. Or, l'environnement utérin module tellement l'expression des gènes que l'animal recréé ne pourrait sans doute pas être classé comme appartenant à l'espèce en question ! Ces chimères isolées risquent donc de devenir des bêtes curieuses, confinées dans des animaleries ou des parcs, ou alors traquées de toutes parts. Ce qui, au demeurant, pourrait être une bonne chose : rien ne dit que ces espèces ressuscitées ne deviennent pas envahissantes si elles parvenaient un jour à trouver leur équilibre !
Apprentis sorciers, ces biologistes ? "De toute évidence, ils n'ont aucune idée précise de ce qu'est l'écologie, critique Pierre-Henri Gouyon. La biodiversité est un processus dynamique qui ne peut pas se congeler !" De fait, les formes du vivant qui nous entourent sont le fruit de plusieurs milliers d'années d'évolution et sont amenées à évoluer encore pour s'adapter aux modifications de l'environnement.
DES PERSPECTIVES FASCINANTES
L'objectif de la conservation n'est donc pas de figer une image romantique ou sauvage de la nature : il s'agit de faire en sorte que sa capacité d'adaptation aux changements soit préservée. Une capacité d'adaptation qui ne peut se recréer en laboratoire.
Au-delà de ces interrogations d'écologues, se pose une autre question : faudrait-il dépenser autant d'argent à sauver certains spécimens disparus alors que tant d'espèces vivantes sont chaque jour un peu plus proches de l'extinction ? "C'est un peu comme si, au milieu d'une grave épidémie mondiale, vous consacriez d'énormes moyens à faire revivre un individu qui vous amuse plutôt que de sauver ceux qui ne sont pas encore morts"... compare Pierre-Henri Gouyon. Et quelles espèces choisir ? Celles exterminées par l'homme, comme le tigre de Tasmanie ? Celles qui nous font le plus rêver ? Celles utiles à l'homme ? Et qui fera ces choix ? Sans compter que ces résurrections pourraient avoir un effet pervers. "En remettant en cause le côté irréversible de la perte d'une espèce, ces nouvelles possibilités risquent d'amenuiser notre responsabilité vis-à-vis de la biodiversité, estime Virginie Maris, philosophe de la biodiversité au Centre d'écologie fonctionnelle et évolutive de Montpellier (CNRS). Il me semble que la crise actuelle de la biodiversité devrait au contraire nous inciter à abandonner cette posture très cartésienne, où l'homme se veut maître et possesseur de la nature".
Maîtres et possesseurs de la nature... Peut-être pas. Mais magiciens du génome, ces biologistes le sont ! En quelques années, la résurrection est passée du domaine de la religion ou de la fiction à la réalité. En promettant de faire revivre un mammouth ou un vélociraptor, les virtuoses de l'ADN concrétisent des rêves, avec de fascinantes perspectives scientifiques sous-jacentes. Il faut vraisemblablement chercher là les vraies motivations de ces biologistes révolutionnaires. Car si la résurrection des morts par la biotechnologie semble à portée de main, aucun miracle n'est à attendre du côté de la conservation...
 QUE FAIRE DE NEANDERTAL S'IL REVENAIT PARMI NOUS ? QUE FAIRE DE NEANDERTAL S'IL REVENAIT PARMI NOUS ?
Selon Georges Church, il serait donc désormais possible de recréer un homme de Neandertal grâce à la technologie de réécriture génétique. Imaginons qu'il ait raison. Imaginons même qu'il parvienne à en recréer un. Qu'en ferions nous ? Irait-il à l'école ? Resterait-il dans un laboratoire ? Une animalerie ?
Bien sûr, les questions que l'on pourrait tester sur cet individu sont fascinantes : depuis le rôle de l'inné et de l'acquis jusqu'à l'apprentissage du langage, en passant par l'influence génétique sur certains comportements sociaux. Mais cela justifie-t-il une telle expérience ? Non, répondent presque unanimes les scientifiques. "Les nouvelles biotechnologies sont souvent jugées immorales jusqu'à ce qu'elles fassent leur preuve, avance de son côté le généticien américain. Si la technique de réécriture génétique s'avère sûre et fiable, elle sera acceptée comme l'a été la fécondation in vitro". Mais dans quel but ? "Recréer des traits génétiques qui pourraient être bénéfiques à la société", répond le chercheur, qui s'appuie sur des travaux tentant de démontrer comment des individus atteints de dyslexie, d'autisme léger ou de désordres bipolaires développent des capacités de compréhension potentiellement utiles, notamment en période de crise. Certains traits propres à Neandertal pourraient-il donc nous servir ? "Cette possibilité stimule les discussions autour de la diversité de fonctionnement cérébral et nous encourage à repenser nos efforts de lutte contre les discriminations sociales", conclut le scientifique, visiblement plus intéressé par ces discussions que par l'idée de donner réellement corps à un Neandertal. Mais le pavé est lancé : on peut désormais le faire. Reste à savoir s'il le faut... |
E.R avec L.B. - SCIENCE & VIE > Décembre > 2011 |
|















