Le Noyau des Atomes |
Des Noyaux Extrêmes Chamboulent la Physique |
E.-O.E. - POUR LA SCIENCE N°555 > Janvier > 2024 |
9 Nucléons dans un Noyau d'Azote Instable |
LE MONDE > 8 Novembre > 2023 |
Le Noyau Atomique : entre Liquide et Cristal |
 Aplati, en poire, plutôt liquide, avec un halo... : le noyau des atomes présente toute une variété de formes et d'états. Une diversité que les physiciens commencent à expliquer.
Aplati, en poire, plutôt liquide, avec un halo... : le noyau des atomes présente toute une variété de formes et d'états. Une diversité que les physiciens commencent à expliquer.
L'ESSENTIEL
- Le noyau atomique présente une grande diversité de formes et de structures.
- La compétition entre le caractère quantique des élémems du noyau et leurs interactions permet de définir trois phases : le liquide quantique, le noyau moléculaire et une phase cristalline.
- Certains noyaux sont constitués en agrégats, tels les atomes dans une molécule. Cet état « moléculaire » a été essentiel dans la formation des éléments tel le carbone.
- La phase cristailine est présente dans les étoiles à neutrons.
La matière qui nous entoure est composée d'atomes, mais à quoi ressemblent-ils ? Héritée du modèle du physiciennéo-zélandais Ernest Rutherford (1871-1937), la représentation la plus courante d'un atome est celle d'un système planétaire microscopique, où des électrons sont en orbite autour d'un noyau sphérique. Avec la mécanique quantique, la représentation s'est affinée en faisant correspondre au cortège électronique un nuage (de densité de probabilité de présence des électrons) plutôt que des orbites. Quant au noyau atomique, est-il vraiment sphérique ? Les physiciens qui l'étudient en ont une image bien plus complexe. Les modèles théoriques et les expériences ont mis en évidence des noyaux aplatis, en bulle, en forme de poire ou de banane, des noyaux dont la structure rappelle celle des molécules, etc.
 Cependant, plus d'un siècle après sa découverte, le noyau atomique n'a pas livré tous ses secrets. Nous ne disposons pas d'une vision globale du noyau qui permette d'expliquer cette diversité de structures dans un cadre unique. Et pour cause, le noyau est un objet quantique difficile à étudier : il est constitué d'éléments eux-mêmes complexes, et trois des quatre forces fondamentales de la nature participent à la dynamique de cet assemblage. L'idée que la variété découle d'un petit nombre de règles fondamentales n'est pas nouvelle. Les chimistes ont ainsi ordonné les éléments dans un tableau en fonction de propriétés qui dépendent du nombre d'électrons sur les couches externes de l'atome. Par ailleurs, les centaines de particules découvertes dans les collisionneurs, répondant au nom de hadrons, ont pu être classées lorsqu'on a compris qu'elles étaient un assemblage de particules élémentaires, les quarks. Pour comprendre la variété des structures du noyau, nous avons donc recherché des règles sous-jacentes et développé une approche théorique qui rend compte des différentes phases du noyau. Similaires aux phases solide, liquide et gazeuse de la matière ordinaire, ces phases dépendent des propriétés de ses composants, les protons et les neutrons. Il est donc essentiel de comprendre la structure du noyau avant d'en étudier les différentes phases.
Cependant, plus d'un siècle après sa découverte, le noyau atomique n'a pas livré tous ses secrets. Nous ne disposons pas d'une vision globale du noyau qui permette d'expliquer cette diversité de structures dans un cadre unique. Et pour cause, le noyau est un objet quantique difficile à étudier : il est constitué d'éléments eux-mêmes complexes, et trois des quatre forces fondamentales de la nature participent à la dynamique de cet assemblage. L'idée que la variété découle d'un petit nombre de règles fondamentales n'est pas nouvelle. Les chimistes ont ainsi ordonné les éléments dans un tableau en fonction de propriétés qui dépendent du nombre d'électrons sur les couches externes de l'atome. Par ailleurs, les centaines de particules découvertes dans les collisionneurs, répondant au nom de hadrons, ont pu être classées lorsqu'on a compris qu'elles étaient un assemblage de particules élémentaires, les quarks. Pour comprendre la variété des structures du noyau, nous avons donc recherché des règles sous-jacentes et développé une approche théorique qui rend compte des différentes phases du noyau. Similaires aux phases solide, liquide et gazeuse de la matière ordinaire, ces phases dépendent des propriétés de ses composants, les protons et les neutrons. Il est donc essentiel de comprendre la structure du noyau avant d'en étudier les différentes phases.
AU COUR DU NOYAU : La vision que l'on a du noyau atomique n'a cessé d'évoluer depuis sa mise en évidence en 1911 par Rutherford. Ce physicien menait alors des expériences pour comprendre la structure de l'atome. Les chercheurs de l'époque savaient que l'atome contenait des électrons, mais il devait renfermer autre chose pour compenser la charge électrique négative des électrons. On pensait l'atome comme un objet de 10-10 mètre de diamètre dans lequel les électrons étaient incrustés, à l'image d'un gâteau contenant des raisins secs. En bombardant une feuille d'or avec des particules a (des noyaux d'hélium) et en mesurant l'angle de déviation des particules rebondissant sur la feuille, Rutherford a compris que l'atome est en réalité constitué d'un minuscule noyau très dense, d'environ 10-15 mètre de diamètre et chargé positivement, accompagné d'un cortège d'électrons 100.000 fois plus étendu que lui.
Le noyau est lui-même un assemblage de «nucléons» : les protons (identifiés par Rutherford en 1917) et les neutrons (découverts en 1932 par James Chadwick). Par la suite, dans les années 1960, les physiciens ont montré que les nucléons sont constitués de particules élémentaires, les quarks et les gluons. Pour l'essentiel, le proton est composé de deux quarks u et un quark d, tandis que le neutron est l'assemblage de deux quarks d et un quark u. La cohésion entre les quarks est assurée par l'interaction forte, véhiculée par des gluons, dont le nom indique leur fonction de colle entre les quarks. C'est également l'interaction forte qui colle les nucléons et maintient la cohésion du noyau. En réalité, la description du nucléon fournie par la chromodynamique quantique - la théorie qui décrit l'interaction forte - est celle d'une «soupe» d'une multitude de quarks et gluons en interaction. Du fait de cette complexité, l'interaction forte entre nucléons n'est que partiellement comprise. Pour compléter ce tableau, il faut ajouter que les protons sont chargés positivement ; par conséquent, la force électromagnétique a une influence dans le noyau. Enfin, les nucléons sont sensibles à l'interaction faible, qui se manifeste par la radio activité bêta, où, par exemple, la transformation d'un neutron en un proton s'accompagne de l'émission d'un électron et d'une autre particule au caractère élusif, le neutrino.
Ainsi, pour étudier le noyau, il faut prendre en compte trois des quatre forces fondamentales (les interactions forte, faible et électromagnétique) et tous ses nucléons. C'est un grand défi d'ordre mathématique. Pourquoi ? Il est assez aisé d'obtenir une description précise d'un système de deux particules en interaction. Il est aussi possible d'étudier statistiquement un système formé d'un très grand nombre d'éléments, un gaz par exemple, et de calculer ses grandeurs thermodynamiques (pression, température, etc.). Cependant, entre ces deux régimes, pour un noyau formé d'une dizaine ou quelques centaines de nucléons, on ne sait décrire le système ni de façon exacte ni de façon statistique. Par exemple, l'ajout d'un seul nucléon à un noyau en bouleverse les propriétés ! Si la complexité du noyau atomique rend son étude très ardue, elle est aussi la source d'une grande diversité de phénomènes touchant la structure du noyau et sa dynamique. Comment intégrer cette variété dans une description fondamentale et unifiée du noyau atomique ? Une approche fructueuse est de considérer que le noyau peut présenter différentes phases qui découlent de la compétition entre la nature quantique des nucléons et leurs interactions. D'après le principe de dualité onde-corpuscule, les nucléons présentent à la fois des propriétés d'onde et de particule. Mathématiquement, ils sont décrits par une fonction d'onde qui détermine leur probabilité de présence : selon que cette fonction est concentrée dans l'espace ou étendue, chaque nucléon est plus ou moins bien localisé dans le noyau. Les interactions des nucléons influent directement sur leur localisation. Plus l'interaction d'un nucléon avec ses congénères domine l'agitation des protons et des neutrons, plus la position du nucléon sera bien déterminée.
 Dans une étude récente, nous avons considéré deux grandeurs caractéristiques du noyau : la dispersion spatiale des fonctions d'onde des nucléons et la distance moyenne entre ces particules. Le rapport de ces deux caractéristiques - le «paramètre de phase» - nous a permis de définir trois phases dans le noyau : liquide, moléculaire et cristalline. Les nucléons y sont plus ou moins localisés, ce qui influe sur la structure, les propriétés et la forme du noyau. Ces phases étaient déjà connues, mais leur description faisait appel à des modèles qui coexistaient, sans que l'on puisse les relier. Il est maintenant possible d'appréhender la diversité des phénomènes observés dans les expériences nucléaires par une approche unique et en partie fixée par le paramètre de phase (schéma ->).
Dans une étude récente, nous avons considéré deux grandeurs caractéristiques du noyau : la dispersion spatiale des fonctions d'onde des nucléons et la distance moyenne entre ces particules. Le rapport de ces deux caractéristiques - le «paramètre de phase» - nous a permis de définir trois phases dans le noyau : liquide, moléculaire et cristalline. Les nucléons y sont plus ou moins localisés, ce qui influe sur la structure, les propriétés et la forme du noyau. Ces phases étaient déjà connues, mais leur description faisait appel à des modèles qui coexistaient, sans que l'on puisse les relier. Il est maintenant possible d'appréhender la diversité des phénomènes observés dans les expériences nucléaires par une approche unique et en partie fixée par le paramètre de phase (schéma ->).
Dans la grande majorité des cas, les nucléons formant le noyau s'organisent dans une phase de liquide quantique. Il faut préciser que les nucléons sont des fermions, c'est-à-dire des particules dont le spin - le moment cinétique intrinsèque - est demi entier (ici 1/2) dans les unités atomiques. Les fermions identiques sont soumis au principe d'exclusion de Pauli qui leur interdit d'être dans un même état quantique. L'approche phénoménologique du liquide quantique a été introduite par le physicien soviétique Lev Landau en 1956. Dans cette phase, l'interaction entre nucléons est importante, mais elle ne suffit pas pour dominer l'agitation de ces derniers. Elle rappelle la phase liquide de la matière ordinaire où les molécules sont en interaction mais où l'agitation thermique reste importante. Comme les interactions des nucléons sont insuffisantes, ceux-ci sont délocalisés dans l'ensemble du volume du noyau. Leurs fonctions d'onde sont très étalées et se recouvrent, ce qui confère au noyau une densité relativement homogène. De telles propriétés autorisent une description du noyau en terme de ce que l'on nomme le champ moyen : un puits de potentiel commun à tous les nucléons capture l'essentiel de la physique du système de nucléons en interaction. Ainsi, dans cette approche, chaque nucléon subit un même potentiel qui résume l'influence des autres particules.
La forme du potentiel nucléaire moyen n'est pas simple à définir, car il faut prendre en compte les spécificités de l'interaction forte et le fait que les nucléons engendrent eux-mêmes ce potentiel. Cette approche a permis de décrire de nombreux phénomènes. Le noyau atomique, dans sa phase de type liquide quantique, présente une grande variété de comportements, comme le laisse supposer la malléabilité propre aux liquides. Ainsi, le noyau peut se déformer lorsqu'il est excité et, parfois, même dans son état de plus basse énergie (non excité), il n'est pas sphérique. Il peut alors adopter des formes exotiques, allant de la soucoupe au ballon de rugby en passant par une forme de poire (observée pour la première fois de façon directe en 2013 grâce à l'installation Isolde au Cern).
DES LIQUIDES QUANTIQUES SUPERFLUIDES : Outre les déformations, le modèle de liquide quantique décrit d'autres propriétés nucléaires. En raison de la nature fermionique des nucléons, on observe dans certains noyaux des corrélations entre deux nucléons. Cela conduit à la formation de paires de fermions, dites de Cooper, et à la superfluidité nucléaire. Ce processus est analogue aux paires de Cooper formées par les électrons dans les métaux supraconducteurs, mécanisme qui conduit à annuler la résistance électrique du matériau. La viscosité du liquide nucléaire diminue drastiquement s'il est superfluide. Cela a un impact sur le moment d'inertie, qui détermine l'énergie du noyau en fonction de sa vitesse de rotation autour de lui-même. Ce phénomène doit être pris en compte lors des mesures en laboratoire. Dans la phase liquide quantique, le puits de potentiel a une profondeur trop faible pour localiser les nucléons dans le noyau. Le paramètre de phase, le rapport de la dispersion spatiale de la fonction d'onde d'un nucléon et de la distance entre deux nucléons voisins, est alors très supérieur à un. Si le potentiel était profond, les nucléons seraient plus localisés, le paramètre de phase diminuerait et l'on tendrait vers une phase cristalline nucléaire, où les nucléons se situeraient aux mailles d'un réseau, comme dans un cristal.
Cette phase cristalline existe-t-elle dans la nature ? Voyons comment le paramètre de phase peut diminuer. Si le nombre de nucléons du noyau augmente, la profondeur du puits de potentiel augmente et le paramètre de phase diminue. Mais on obtient rapidement un effet de saturation, conséquence de la courte portée des forces s'exerçant entre les nucléons : la profondeur du puits de potentiel atteint une valeur limite quasi indépendante du noyau considéré. Par ailleurs, on montre que la dispersion spatiale de la fonction d'onde augmente avec le nombre de nucléons. Finalement, un noyau riche en nucléons aura un comportement de liquide quantique et un paramètre de phase supérieur à un. Un noyau léger ne contient pas suffisamment de nucléons pour former une structure cristalline. Cet état ne semble donc pas possible dans un noyau atomique.
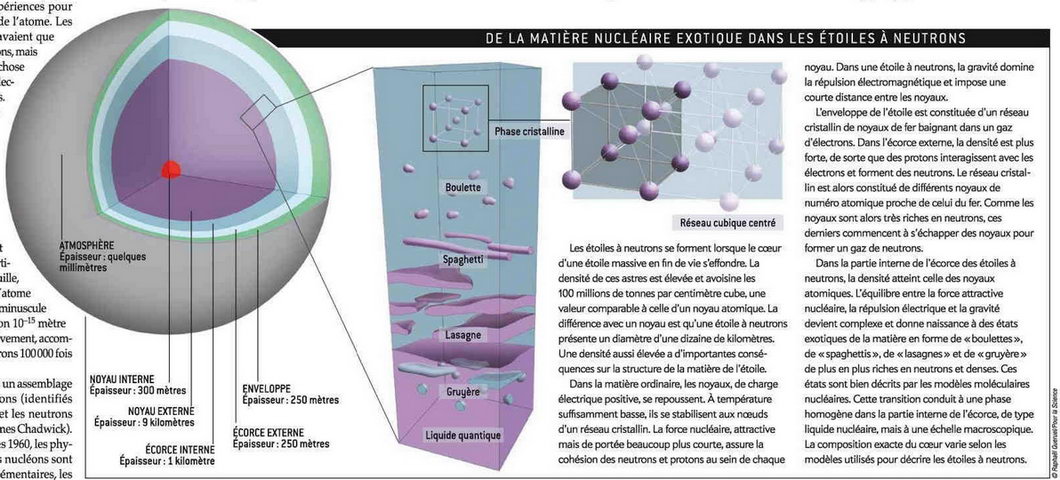 En revanche, il pourrait exister dans l'écorce des étoiles à neutrons. Prédites peu après la découverte du neutron dans les années 1930, ces étoiles sont restées hypothétiques jusqu'à ce que, en 1967, Jocelyn Bell, une doctorante, découvre les pulsars, caractérisés par une émission radio d'une période allant de quelques dizaines de millisecondes à quelques secondes. Un pulsar est une étoile à neutrons en rotation rapide émettant un jet qui balaie l'espace de façon périodique, comme un phare. On en a observé quelques milliers à l'heure actuelle. De masse comparable à celle du Soleil mais avec un rayon d'une dizaine de km, les étoiles à neutrons sont parmi les objets les plus denses de l'Univers : un cm³ d'un tel astre pèse environ 100 millions de tonnes. Cette densité extrême est comparable à celle des noyaux atomiques. Ce lien entre la physique du noyau et l'astrophysique conduit à modéliser les étoiles à neutrons comme des sortes de noyaux géants. Or on calcule que les effets gravitationnels très intenses imposent dans les couches externes de ces étoiles une densité qui conduit à l'apparition de cristaux nucléaires (schéma ->).
En revanche, il pourrait exister dans l'écorce des étoiles à neutrons. Prédites peu après la découverte du neutron dans les années 1930, ces étoiles sont restées hypothétiques jusqu'à ce que, en 1967, Jocelyn Bell, une doctorante, découvre les pulsars, caractérisés par une émission radio d'une période allant de quelques dizaines de millisecondes à quelques secondes. Un pulsar est une étoile à neutrons en rotation rapide émettant un jet qui balaie l'espace de façon périodique, comme un phare. On en a observé quelques milliers à l'heure actuelle. De masse comparable à celle du Soleil mais avec un rayon d'une dizaine de km, les étoiles à neutrons sont parmi les objets les plus denses de l'Univers : un cm³ d'un tel astre pèse environ 100 millions de tonnes. Cette densité extrême est comparable à celle des noyaux atomiques. Ce lien entre la physique du noyau et l'astrophysique conduit à modéliser les étoiles à neutrons comme des sortes de noyaux géants. Or on calcule que les effets gravitationnels très intenses imposent dans les couches externes de ces étoiles une densité qui conduit à l'apparition de cristaux nucléaires (schéma ->).
 Ces étoiles pourraient héberger d'autres formes exotiques de la matière. Leur écorce présente une structure cristalline tandis que le noyau interne est décrit comme un liquide quantique nucléaire de plusieurs km de rayon. Entre ces deux régions, il existerait une phase hybride de type «molécule nucléaire». Cette phase se caractérise par une dispersion de la fonction d'onde des nucléons du même ordre de grandeur que la distance moyenne qui les sépare (le paramètre de phase vaut environ un). Cette phase moléculaire existe aussi dans certains noyaux formés de quelques dizaines de nucléons. Ces noyaux gagnent en stabilité lorsque les nucléons se regroupent en agrégats chacun formant une particule a (deux protons et deux neutrons). Ces noyaux moléculaires rappellent les molécules classiques constituées d'atomes, à la différence que les noyaux moléculaires sont 100.000 fois plus petits. En outre, les noyaux ayant peu de protons, mais un excédent de neutrons, ils développent facilement une structure en agrégats : les neutrons excédentaires, faiblement liés, se délocalisent entre les agrégats et jouent le même rôle stabilisateur que les électrons dans les liaisons de valence entre les atomes d'une molécule. L'idée d'un noyau structuré en agrégats de nucléons remonte aux années 1930, quand les physiciens américains Lawrence Hafstad et Edward Teller ont proposé que les noyaux de béryllium 8, carbone 12, oxygène 16 et néon 20, qui ont autant de protons que de neutrons, pouvaient être décrits par des assemblages de particules a.
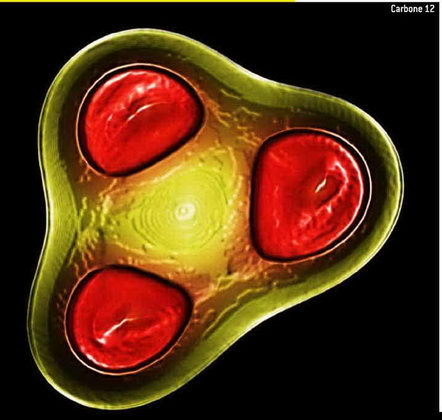
Ces étoiles pourraient héberger d'autres formes exotiques de la matière. Leur écorce présente une structure cristalline tandis que le noyau interne est décrit comme un liquide quantique nucléaire de plusieurs km de rayon. Entre ces deux régions, il existerait une phase hybride de type «molécule nucléaire». Cette phase se caractérise par une dispersion de la fonction d'onde des nucléons du même ordre de grandeur que la distance moyenne qui les sépare (le paramètre de phase vaut environ un). Cette phase moléculaire existe aussi dans certains noyaux formés de quelques dizaines de nucléons. Ces noyaux gagnent en stabilité lorsque les nucléons se regroupent en agrégats chacun formant une particule a (deux protons et deux neutrons). Ces noyaux moléculaires rappellent les molécules classiques constituées d'atomes, à la différence que les noyaux moléculaires sont 100.000 fois plus petits. En outre, les noyaux ayant peu de protons, mais un excédent de neutrons, ils développent facilement une structure en agrégats : les neutrons excédentaires, faiblement liés, se délocalisent entre les agrégats et jouent le même rôle stabilisateur que les électrons dans les liaisons de valence entre les atomes d'une molécule. L'idée d'un noyau structuré en agrégats de nucléons remonte aux années 1930, quand les physiciens américains Lawrence Hafstad et Edward Teller ont proposé que les noyaux de béryllium 8, carbone 12, oxygène 16 et néon 20, qui ont autant de protons que de neutrons, pouvaient être décrits par des assemblages de particules a.  Il faudra attendre les années 1960 pour voir l'élaboration des premiers outils théoriques dédiés à leur description et la mise en place d'expériences les révélant. C'est ainsi que l'on découvrit que les noyaux légers ayant un nombre égal de protons et de neutrons ont tendance à exhiber des agrégats de nucléons dans leurs états excités. L'existence du carbone 12 est la meilleure preuve que certains noyaux sont dans la phase moléculaire (encadré ->). La synthèse de cet élément dans les étoiles passe par une réaction clé : la fusion de trois particules a qui produit un état excité, décrit comme un état moléculaire de trois particules a et nommé état de Hoyle. Sans la formation de cet état excité, la synthèse du carbone, de l'oxygène et de tous les éléments plus lourds serait bloquée.
Il faudra attendre les années 1960 pour voir l'élaboration des premiers outils théoriques dédiés à leur description et la mise en place d'expériences les révélant. C'est ainsi que l'on découvrit que les noyaux légers ayant un nombre égal de protons et de neutrons ont tendance à exhiber des agrégats de nucléons dans leurs états excités. L'existence du carbone 12 est la meilleure preuve que certains noyaux sont dans la phase moléculaire (encadré ->). La synthèse de cet élément dans les étoiles passe par une réaction clé : la fusion de trois particules a qui produit un état excité, décrit comme un état moléculaire de trois particules a et nommé état de Hoyle. Sans la formation de cet état excité, la synthèse du carbone, de l'oxygène et de tous les éléments plus lourds serait bloquée.
LE HALO : DES NEUTRONS TRÈS DÉLOCALISÉS ; Notre approche fondée sur le paramètre de phase a permis de classer un grand nombre de configurations nucléaires selon trois phases. Ainsi, les noyaux riches en nucléons forment des liquides quantiques, tandis que les noyaux légers présentent parfois un comportement moléculaire. Cependant, les noyaux atomiques peuvent se trouver dans d'autres états exotiques, tels les halos. En 1985, Isao Tanihata et ses collègues ont mesuré le rayon de plusieurs noyaux légers au Laboratoire Lawrence Berkeley, aux États-Unis. Le lithium 11 a un diamètre comparable à celui du plomb 208, alors qu'il a 20 fois moins de nucléons. Ce noyau est doté d'un halo formé par deux neutrons très délocalisés.
D'autres noyaux riches en neutrons exhibent aussi une structure de halo. Cette délocalisation de la fonction d'onde de certains nucléons dans les noyaux à halo provient de leur faible énergie de liaison. Plusieurs observations directes de noyaux à halo ont été réalisées dans différents laboratoires dans le monde, comme au Ganil (Grand Accélérateur national d'ions lourds) en France. L'état de halo s'intègre dans notre description unifiée des divers états nucléaires. Il serait un cas extrême de délocalisation de la fonction d'onde de certains nucléons. La difficulté expérimentale pour étudier de nouvelles formes nucléaires est qu'elles apparaissent dans des noyaux instables, dont la durée de vie est de l'ordre de quelques nanosecondes à quelques millisecondes. Ces noyaux se désintegrent en effet rapidement par interaction faible. Il en est ainsi pour les noyaux bulles, sortes de noyaux creux prédits par les théoriciens. La déplétion de matière en leur cour est due à un effet spécifiquement quantique : la probabilité de présence des protons au centre du noyau est très faible - un effet surprenant, le cour des noyaux atomiques étant en général ultradense. Cet état serait un cas particulier des liquides quantiques. Certains indices expérimentaux de l'existence de noyaux bulles ont récemment été obtenus au Ganil. La prochaine étape consiste à mettre en évidence de façon directe le creux de matière au sein de ces noyaux, dont un candidat est le silicium 34 instable.
 Les noyaux instables représentent 95 % des édifices nucléaires connus, alors que les noyaux stables, tel celui de l'oxygène que nous respirons, n'en constituent que 5 %. La physique nucléaire du XXè siècle a été marquée par l'étude des 300 noyaux stables et a ouvert la voie à l'étude des noyaux instables. Les expériences de notre siècle s'orientent vers une étude systématique de ces derniers, qui se comptent par milliers. Les installations les plus récentes (ou en construction) au Japon, aux Etats-Unis et en Europe (France, Allemagne, Cern) permettront de se rapprocher de la limite théorique d'existence des noyaux, dont on estime le nombre total à environ 7000. Nous découvrirons alors peut-être de nouveaux états de la matière qui nécessiteront d'affiner nos modèles, voire des formes et états que les physiciens n'ont pas encore imaginés.
Les noyaux instables représentent 95 % des édifices nucléaires connus, alors que les noyaux stables, tel celui de l'oxygène que nous respirons, n'en constituent que 5 %. La physique nucléaire du XXè siècle a été marquée par l'étude des 300 noyaux stables et a ouvert la voie à l'étude des noyaux instables. Les expériences de notre siècle s'orientent vers une étude systématique de ces derniers, qui se comptent par milliers. Les installations les plus récentes (ou en construction) au Japon, aux Etats-Unis et en Europe (France, Allemagne, Cern) permettront de se rapprocher de la limite théorique d'existence des noyaux, dont on estime le nombre total à environ 7000. Nous découvrirons alors peut-être de nouveaux états de la matière qui nécessiteront d'affiner nos modèles, voire des formes et états que les physiciens n'ont pas encore imaginés.
J.-P.E. et E.K. - POUR LA SCIENCE N°448 > Février > 2015 |
Le Noyau Atomique est à la fois Liquide et Solide |
 Des chercheurs Français et croates ont résolu, en s'appuyant sur les solutions de l'équation de Schrödinger, une contradiction de la physique moléculaire.
Des chercheurs Français et croates ont résolu, en s'appuyant sur les solutions de l'équation de Schrödinger, une contradiction de la physique moléculaire.
Repères : Le noyau atomique est fait de nucléons - neutrons et protons- maintenus ensemble par l'intéraction forte. Le noyau d'hydrogène ne possède qu'un proton tandis que celui du plus lourd des éléments naturels, l'uranium, renferme 92 protons et 146 neutrons.
Les plus légers seraient comparables à de minuscules agrégats rigides tandis que les plus lourds ressembleraient à une goutte de liquide : les physiciens avaient jusque là deux images apparemment contradictoires pour décrire la nature d'un seul et même objet, le noyau atomique. Or, elles ne sont pas incompatibles, révèlent Jean-Paul Ebran, du Commissariat à l'énergie atomique (CEA), et Elias Khan, de l'Institut de physique nucléaire d'Orsay, avec leurs collègues de l'université de Zagreb (Croatie). Comment font les physiciens pour saisir la nature de cet amas de nucléons d'à peine un millionième de milliardième de mêtre ? Ils recourent à la physique quantique, qui propose une vision probabiliste de la matière : ainsi, on évoque la probabilité de présence d'une particule plutôt que sa position. Et à des modèles, seuls capables de décrire ce qui se passe a l'échelle subatomique.
Les deux modèles proposés permettaient justement d'expliquer à merveille comment les atomes les plus légers ont été synthétisés dans les étoiles et, l'inverse, pourquoi les plus lourds ont tendance à se fractionner (ce qu'on appelle la fission), comme le ferait une goutte trainée sur une surface. Pour les concilier, les chercheurs ont examiné les solutions de l'équation de Schrödinger qui décrit, en physique quantique, l'évolution d'une particule au repos. Et vu ainsi comment s'effectue le passage d'un modèle à l'autre. "À mesure que le mombre de nucléons et la taille du noyau augmentent, les intéractions entre neutrons et protons ne sont plus assez fortes pour fixer les nucléons au sein du moyau, explique Elias Khan. Celui-ci devient alors comme un liquide, avec des nucléons délocalisés. À l'inverse, dans un petit noyau, les nucléons sont maintenus de manière plus rigide". Avec la physique quantique, le noyau de l'atome était devenu insaisissable : le voici maintenant dual. Une situation qui rappelle ce qu'on observe dans les... étoiles à neutrons ! Lorsqu'une étoile explose, elle expulse en effet ses couches superficielles tandis que son cour s'effondre sur lui-même par l'action de la gravité, ce qui produit un astre extraordinairement lourd, forme de neutrons maintenus par la gravité. Or, dans ces étoiles à neutrons, la matière passe progressivement d'un état de solide cristallin en surface à un état liquide en profondeur.
A.KH. - SCIENCES ET AVENIR N°787 > Septembre > 2012 |
La Vallée de la Stabilité et Au-Delà |
 Décortiqués, triturés, fracassés dans les accélérateurs de particules, les noyaux des atomes se révèlent plus exotiques qu'on ne l'imaginait. Chacun des 92 éléments chimiques de notre planète possède un noyau unique par son nombre de protons et d'électrons.
Décortiqués, triturés, fracassés dans les accélérateurs de particules, les noyaux des atomes se révèlent plus exotiques qu'on ne l'imaginait. Chacun des 92 éléments chimiques de notre planète possède un noyau unique par son nombre de protons et d'électrons.
ATOMES
Ils sont formés d'un nuage d'électrons - des particules portant une charge électrique négative - qui entourent un noyau constitué de deux types de particules, les protons, chargés positivement, et les neutrons, sans charge électrique. L'atome est habituellement neutre, car la charge des protons compense celle des électrons.
La croûte terrestre en compte 92, qui ont chacun un nombre d'électrons et un noyau bien spécifiques. Ils sont habituellement classés dans un tableau théorique standard - dit table de Mendeleïev, du nom du chimiste russe qui en a inventé le principe en 1869 - par ordre croissant du nombre d'électrons, depuis le plus simple, l'atome d'hydrogène (un électron, un proton) jusqu'à l'uranium 235 (92 électrons, 92 protons et 143 neutrons). Chacun possède son symbole, en général les deux premières lettres de l'élément... mais attention à l'azote (N pour nitrogen) ou à l'antimoine (Sb, stibium en grec) !
À gauche de ce symbole, deux chiffres : en bas, le nombre de charge (Z) qui représente le nombre de protons du noyau (ou son nombre d'électrons, puisque l'atome est neutre), en haut le nombre de masse (A), qui est la somme des nucléons (neutrons plus protons). Quant au chiffre à droite, il indique la masse moyenne des isotopes de l'élément.
ISOTOPES
Certains éléments existent naturellement en plusieurs variétés, des isotopes, qui ont le même nombre d'électrons et donc les mêmes affinités chimiques, mais diffèrent par leur nombre de neutrons.
Ainsi, le carbone existe dans la nature sous la forme de trois isotopes : le 12C, le 13C et le 14C, tous ayant 6 électrons et 6 protons, mais respectivement 6, 7 et 8 neutrons. 12C et 13C sont stables, leur noyau est à peu près sphérique. En revanche, le carbone 14C, instable, est radioactif.
NOYAUX STABLES ET NOYAUX RADIOACTIFS
Les physiciens disposent les noyaux dans un graphe (ci-dessus) où le nombre de protons (Z) est présenté en fonction du nombre de neutrons (N). La droite médiane correspond donc aux noyaux qui possèdent ces particules en nombre égal. Les éléments chimiques les plus stables apparaissent en blanc et forment ce que l'on appelle la vallée de la stabilité : elle suit la médiane pour les éléments chimiques les plus légers, puis s'en écarte au fur et à mesure que le numéro atomique augmente. Un peu à l'écart de cette vallée, se trouvent des noyaux étonnamment stables à cause de la disposition de leurs nucléons : les noyaux magiques. De part et d'autre de cette vallée de la stabilité, se situent les noyaux que l'on cherche à créer au Ganil. Leur nombre de neutrons excède leur nombre de protons. Plus ils s'éloignent de la vallée, moins ils durent. A peine formés, ils disparaissent en éjectant un proton ou un neutron, par radioactivité... et la rejoignent aussitôt ! Aujourd'hui c'est l'élément 83, le bismuth, qui occupe le haut de la zone en blanc. Mais un îlot de stabilité pourrait exister autour de l'élément 124.
A.Kh. - SCIENCES ET AVENIR Hors Série > Mai > 2010 |
Ganil : les Forgerons de la Matière |
Pour mieux connaître les noyaux des atomes, les chercheurs en fabriquent eux-mêmes. De plus en plus lourds. Et parfois magiques !
Des kilomètres de boyaux enchevétrés relient entre elles de grosses et mystérieuses machines : ici des aimants, là une suite d'écrans, plus loin l'unité de contrôle, tandis que dans la pièce à côté, un détecteur ventre ouvert est en cours de maintenance. Nous voilà dans un drôle de temple dédié à un objet un milliard de fois plus petit qu'un cheveu : le noyau de l'atome. Non pour en faire du combustible et produire de l'énergie, comme dans une centrale nucléaire, mais afin de connaître ses ultimes secrets. Au Grand Accélérateur national d'ions lourds (Ganil), à Caen, se rencontrent les membres de la grande confrérie de la physique nucléaire : ceux qui élaborent des théories sophistiquées pour imaginer la structure intime du noyau et ceux qui ont décidé de le briser, le projeter, l'émietter, pour en recueillir les fragments et les analyser. Ou encore de le triturer pour tester sa stabilité. Question : comment peut-on manipuler cet infiniment petit de la nature ? Grâce à l'outil-phare des physiciens, le cyclotron, alias accélérateur. Mais ici, à la différence du Cern, on ne propulse pas des particules, mais directement un atome qui a perdu quelques-uns de ses électrons. Ceux-ci, grâce à leur charge négative, compensent habituellement la charge positive des protons (article La Vallée de la Stabilité précédent). Sans eux, l'atome n'est plus neutre et devient ce qu'on appelle un "ion". Dès cet instant, placé entre les mâchoires d'un aimant, il effectue comme toute particule chargée une trajectoire circulaire, accélère, acquérant ainsi une énergie de plus en plus grande. La collision avec un autre noyau sera d'autant plus "juteuse" aux yeux des physiciens : les deux noyaux se fragmenteront pour en former un nouveau, tout en laissant échapper une grande partie de leurs "ingrédients". Le noyau ainsi obtenu sera plus gros, au point de devenir "exotique", c'est-à-dire plus lourd que ceux existant dans la nature.
DES BILLES ET DE LA GLU
Car la croûte terrestre ne présente que 92 éléments chimiques, atomes qui diffèrent les uns des autres par leur quantité de particules. Ces éléments portent chacun un numéro, en fonction du nombre de neutrons présents dans leur noyau : de 1 (pour l'hydrogène) jusqu'à 92 (pour l'uranium). "Dans les quelques accélérateurs d'ions du monde, nous avons réussi à obtenir des éléments de plus en plus lourds. Dernier en date, l'élément chimique 118", précise Hervé Savajols, du CNRS. Son nom ? "Imprononçable ! Ununoctium", ce qui, en "latin bricolé de laboratoire", signifierait "118". Russes et Américains l'ayant découvert conjointement, les uns militaient pour Moscovium et les autres pour Ghiorsium, du nom du directeur de l'équipe. L'Union internationale pour la chimie pure et appliquée, instance officielle qui attribue les noms d'éléments, s'est prudemment abstenue... De même, le 116 se nomme "ununhexium".
Pas la peine de demander à quoi ressemblent ces poids très lourds : nul n'a eu le temps d'en prélever une poignée. Aussitôt apparus, ils ont disparu : leur durée de vie n'excède pas quelques millisecondes. Cependant, ce n'est pas pour figurer au Grand Livre des records que les laboratoires du monde entier se sont lancés dans cette course au plus lourd élément. L'assemblage de base de notre monde, à savoir le noyau de l'atome, est encore largement inconnu, et la meilleure manière de l'explorer, c'est de tenter d'en fabriquer soi-même.
"Tout se passe comme s'il fallait former une boule - le noyau - faite d'un grand nombre de petites billes, explique Hervé Savajols. Nous disposons de deux sortes de billes, les neutrons et les protons. Une sorte de glu naturelle - l'interaction forte - les maintient ensemble. Nous explorons les très nombreuses possibilités que nous offre ce jeu, à la manière des enfants qui tentent parfois d'empiler un maximum de cubes avant que la tour ne s'effondre. Nous nous demandons combien de billes on peut maintenir ensemble. Au bout de combien de temps la boule formée d'un très grand nombre de billes perdra sa cohésion. Quelle est la recette de la stabilité. Autant de neutrons que de protons, ou l'un des deux doit-il être en excès ?"
La réponse est parfois pleine de surprises : a priori, au fur et à mesure que l'on augmente le nombre de billes, l'édifice devrait s'effondrer. Comment expliquer alors que l'élément 105 tienne 16 heures avant de voir la moitié de ses ingrédients se décomposer, alors que l'élément 104 ne tient qu'une heure avant de subir une désintégration radioactive ? Pourquoi les éléments 20 ou 28 sont-ils bien plus stables que le 18 ou le 19 ? "Noyaux magiques !", répond Jean-Charles Thomas, qui a mené son travail de thèse sur l'un de ces noyaux découverts au Ganil. Rien d'ésotérique dans cette appellation : "C'est ainsi que nous désignons les noyaux les plus stables". Mais pourquoi le 20 et pas le 19, par exemple ? Bref, qu'est-ce qui explique cette loterie ? "Les nucléons ne sont pas disposés n'importe comment dans le noyau. En réalité, ils se placent sur des niveaux d'énergie différents de façon stricte", explique Jean-Charles Thomas. Résultat : à chaque fois qu'un niveau est complètement rempli, on forme un édifice atomique très stable. Ainsi les théoriciens qui ont dans leurs cartons quelques modèles du noyau font-ils des paris sur les futurs noyaux magiques. Le prochain tombera-t-il dans l'escarcelle du Grand Accélérateur ? "Il ne s'appellera peut-être pas "ganilium", mais nous avons bon espoir d'atteindre des éléments chimiques entre 120 et 124", précise Sydney Gales, directeur du Ganil. C'est justement autour de 124 que les théoriciens prédisent le futur noyau magique sur la liste. S'il pointe son nez, il apportera la preuve de la solidité du modèle actuel.
1015 PARTICULES PAR SECONDE
Pour atteindre ces noyaux poids lourds, le Ganil devrait encore s'étendre d'ici 2012 afin d'abriter une nouvelle machine, Spiral 2, la plus puissante d'Europe. En tout, les installations occuperont le double de l'emplacement actuel. Le financement sera assuré à 50 % par le CEA, le CNRS et la région Basse-Normandie, tandis qu'une collaboration internationale - à laquelle participeront le département de l'Energie des Etats-Unis, l'Inde, la Bulgarie et la Pologne - assurera le complément. "Avec Spiral 2, les faisceaux injecteront 1015 particules par seconde, soit cent fois plus que la puissance des machines actuelles", promet Sydney Gales.
RADIOACTIVITÉ ALPHA ET BÊTA Qu'arrive-t-il à l'armée de noyaux exotiques créés au Ganil ? Aussitôt apparus, ils deviennent radioactifs et se transforment en d'autres éléments. Ce phénomène, courant dans la nature, est lié à l'instabilité des noyaux dont le nombre de neutrons est très différent de celui des protons. Plus l'écart est grand, plus la durée de vie des noyaux est courte. Résultat : pour devenir stable, ils se débarrassent rapidement de nucléons (neutron ou proton) en émettant un rayonnement. Les noyaux ont deux façons d'abandonner des nucléons indésirables. Parfois, deux neutrons et deux protons sont éjectés en même temps : c'est la radioactivité alpha, à l'issue de laquelle la nature du noyau change. Ainsi le polonium 210 (84 protons et 126 neutrons) devient du plomb 206 (82 protons et 124 neutrons). La radioactivité bêta, quant à elle, survient lorsqu'au sein d'un noyau, un proton se change en neutron ou vice versa : ce changement aboutit à l'émission d'un électron (ou d'un positon, antiparticule de l'électron) et d'un neutrino (ou d'un antineutrino). Par exemple, le potassium 40 (19 protons et 21 neutrons) se transforme en calcium 40 (20 protons et 20 neutrons). Quant à la mutation du carbone 14 (6 protons et 8 neutrons) en azote 14 (7 protons et 7 neutrons), elle a permis la mise au point de la datation dite "au carbone 14". Explication : un arbre absorbe continuellement du carbone 14. Lorsqu'il meurt, la quantité de carbone qu'il contient se fige, puis décroît au cours du temps, à vitesse constante. En mesurant la quantité d'élément père restant et celle d'élément fils formé, on peut estimer l'âge du bois. |
Les poids lourds ne seront pas les seuls à voir tester leur stabilité. Car la première question que se posent les scientifiques est simple : pourquoi certains des 92 éléments naturels se présentent-ils sous la forme de plusieurs variétés, que l'on nomme isotopes, ne différant l'une de l'autre que par leur nombre de neutrons ? Ainsi, le carbone. Dans la nature, il existe à 98,89 % sous la forme de carbone 12, celui qui rentre dans la constitution du vivant, alors que 1,1 % est du carbone 13. Similaire en tout point à son frère, il comporte simplement un neutron en plus : il est donc un peu plus lourd, mais toujours stable. Enfin, seulement 10-12 (mille milliardièmes) du carbone correspondent au carbone 14 (deux neutrons en plus que le 12) qui est, lui, radioactif, et utilisé comme tel pour la datation (encadré ci-dessus). Pourquoi, d'ailleurs, certains éléments sont-ils radioactifs, leur quantité diminuant au cours du temps, tandis que d'autres ne bougent pas d'un iota ? "Selon les théories, près de 6000 noyaux différents ont existé à un moment ou à un autre dans l'Univers, explique Hervé Savajols. Ils apparaissent au sein de processus très violents : explosion d'étoile en fin de vie, par exemple, ou encore collision entre deux étoiles à neutrons... Or, en laboratoire, nous n'avons pu en produire que 2000, dont seuls 290 ayant une durée de vie plus grande que l'âge de la Terre, c'est-à-dire 4,5 milliards d'années. Plus de la moitié des noyaux théoriquement prévus n'ont encore jamais été observés".
Il faut dire que certains ne tiennent que 10-21 secondes avant de se transformer dare-dare en l'un de ces 290 qui affichent une stabilité à toute épreuve ! Les noyaux qui ont la plus grande longévité forment pour les physiciens la vallée de la stabilité", mais il faut quitter sa vallée pour faire des incursions au sein des éléments exotiques qui ne vivent pas bien longtemps... Ces explorations se font dans trois directions : du côté des éléments de plus en plus lourds, comme on l'a vu, puis, pour un même élément stable, du côté des isotopes de plus en plus riches en neutrons, et vers les éléments de plus en plus riches en protons. "Pour y parvenir, trois procédés : soit un faisceau de noyaux lourds est projeté vers une cible et se fragmente, donnant naissance à toutes sortes de noyaux exotiques, soit deux noyaux légers projetés l'un contre l'autre fusionnent pour en former un plus lourd, soit, enfin, un élément lourd se fissionne, c'est-à-dire se partage en deux noyaux exotiques", précise Jean-Charles Thomas. Or, les installations existantes étaient insuffisantes pour atteindre les noyaux les plus exotiques de cette terra incognita à la limite de la stabilité nucléaire. D'où la nécessité de bâtir Spiral 2.
AU SEIN DES SUPERNOVÆ
Pour l'heure, le noyau recèle encore bien des secrets. Peut-il grossir indéfiniment lorsqu'on le bombarde de neutrons ? Autrement dit, lorsqu'on fait capturer des neutrons par un noyau qui en possède déjà beaucoup, ce qui permet de produire des éléments encore plus lourds ? "C'est ainsi par exemple que se forment les éléments chimiques plus lourds que le fer au sein des supernovae, ce phénomène qui accompagne l'explosion d'une étoile, explique Hervé Savajols. Sauf qu'à partir d'un certain moment, à force d'augmenter le nombre de neutrons, le noyau finit par prendre une allure dissymétrique. Les forces de cohésion interne ne parviennent plus à opérer. C'est là que des phénomènes inconnus apparaissent. Prenons le noyau de l'atome de lithium. Dans la nature, il possède trois protons et trois neutrons. Mais nous avons créé un lithium capable de supporter artificiellement jusqu'à 8 neutrons, et qui parvient à subsister quelques dizaines de millisecondes. Un temps très long, vu sa dissymétrie. Y a-t-il d'autres surprises de ce type, et pourquoi ? Nous ne le savons pas encore".
Si, à l'inverse, on rajoute des protons, c'est un autre scénario qui se produit : ces particules chargées positivement se repoussent. Quelle quantité de protons peut-on ajouter avant que le noyau ne se désintègre spontanément en les expulsant par radioactivité ? "Nous n'aurons pas la réponse avant d'avoir exploré au-delà de la vallée de la stabilité"... Mais toute la chimie du monde - le fait que l'oxygène, élément indispensable à la vie, soit un noyau très stable, ou que le silicium existe en si grande quantité à la surface de la Terre - dépend de deux processus nucléaires : la capture d'un neutron ou le largage d'un proton. Lequel des deux l'emporte le plus souvent ? C'est la question de la prochaine décennie !
A.K. - SCIENCES ET AVENIR Hors Série > Mai > 2010 |
Excentriques Noyaux Exotiques |
 Dans leurs escapades loin du monde harmonieux des noyaux stables, les chercheurs du Ganil vont de surprise en surprise.
Dans leurs escapades loin du monde harmonieux des noyaux stables, les chercheurs du Ganil vont de surprise en surprise.
Bananes, pommes, poires... on trouve de tout au Ganil ! Les noyaux traqués par les physiciens - ceux qui n'existent pas à l'état naturel sur Terre mais pourraient apparaître ça et là dans les étoiles qui explosent ou les trous noirs qui s'entrechoquent - ont parfois des formes rappelant les fruits du verger. D'autres ressemblent à de véritables guimauves : là où les chercheurs pensaient trouver une boule compacte, ils découvrent un loukoum distendu. Certains, encore, changent de forme et naviguent entre sphère et soucoupe volante. Mais ces surprises sont réjouissantes : elles montrent que l'histoire est loin d'être terminée et que la physique nucléaire regorge encore d'énigmes...
Dans les premières décennies du XXe siècle, les noyaux de l'atome sont décrits comme des gouttes liquides. Ce modèle a permis de calculer leur forme sans parvenir à expliquer la stabilité de certains et la vie très éphémère de beaucoup. Dans les années 1950, la physicienne américaine Maria Goeppert-Mayer, prix Nobel 1963, propose un autre modèle : le noyau se présente comme une sphère dense au sein de laquelle neutrons et protons sont disposés sur des couches concentriques, en pelures d'oignon. Chaque couche n'admet qu'un nombre précis de protons et de neutrons : 2 nucléons pour la première couche au cour de la sphère, puis 6 sur la seconde, 12 sur la suivante... Bien rond, bien équilibré, avec un ordre quasi militaire, ce modèle d'atome ne permet cependant pas d'expliquer pourquoi certains, appelés magiques (lire plus haut), sont très stables. Résultat : les physiciens nucléaires continuent de buter sur les subtilités du noyau. Il faut dire qu'elles sont nombreuses... Pour commencer, les ingrédients qui le composent ont chacun leur originalité : les neutrons, comme leur nom l'indique, sont neutres, alors que les protons ont une charge électrique positive. Le noyau comportant habituellement plusieurs protons, ils devraient, étant de charge électrique de même signe, se repousser mutuellement selon "la répulsion coulombienne", force quantifiée pour la première fois au XVIIIe siècle par Charles-Augustin de Coulomb. Si le noyau tient, c'est parce que la répulsion est contrebalancée par l'interaction forte, une force attractive qui s'exerce entre deux nucléons.
Si l'on schématise la représentation du noyau sans tenir compte des effets quantiques, on peut dès lors imaginer facilement la disposition la plus solide : mieux vaut que deux protons mitoyens, dont la répulsion affaiblit la cohésion du noyau, soient séparés par un neutron. Intercaler neutrons et protons pourrait ainsi devenir la règle d'or de la cohésion du noyau. Un agencement aisé pour les noyaux légers qui ne possèdent pas beaucoup d'ingrédients. Mais dès que le nombre de nucléons devient important, la probabilité que plusieurs protons se trouvent côte à côte augmente aussi. "Ainsi, plus les éléments sont lourds, plus le noyau doit comporter de neutrons pour garantir leur stabilité", précise Hervé Savajols, du Ganil. Mais, comme toujours, cette règle ne peut fonctionner sans exception. Car au-delà des deux forces en compétition, la répulsion coulombienne et l'interaction forte, les effets de la mécanique quantique sévissent aussi dans le noyau... En 1925, Wolfgang Pauli annonçait son principe d'exclusion : deux nucléons ne peuvent se trouver dans le même état quantique. Résultat : l'excès de neutrons a aussi ses limites, car fatalement, il conduit à un trop grand nombre de particules dans le même état. Les modèles théoriques n'ont donc pas encore dit le dernier mot. Seule solution : avancer à tâtons et explorer les noyaux les uns après les autres.
Au cours de leurs escapades en dehors de la "vallée de la stabilité", les physiciens du Ganil sont ainsi allés de surprise en surprise. D'abord, certains noyaux bien éloignés du val fertile forment un point de stabilité isolé. "Ces noyaux magiques ont un nombre de protons ou de neutrons tel qu'ils doivent être disposés d'une manière particulière, s'organiser en couches bien remplies et compactes, explique Hervé Savajols. Ce qui augmente leur stabilité". Si l'on croit les modèles théoriques, le prochain du genre est à rechercher du côté du noyau magique superlourd 126.
DISSIDENCES NUCLÉAIRES
Ces noyaux magiques ont la particularité d'être bien sphériques. Ce n'est pas le cas de certains autres : à cause de couches partiellement remplies, leur noyau se déforme de façon non homogène. Parfois, la déformation est si grande que le noyau apparaît deux fois plus long que large : on dit qu'il est superdéformé. Ces déformations extrêmes peuvent entraîner la fission du noyau, sa brisure en deux fragments. Selon le remplissage des couches, les noyaux deviennent banane, cigare, ovni... La compacité n'est pas le propre de tous les noyaux. Prenez par exemple le lithium 11 : son noyau contient 3 protons et 8 neutrons, donc en tout et pour tout 11 nucléons. Imaginez la surprise des chercheurs lorsqu'ils ont découvert que ce minus occupait un volume plus grand que le noyau du plomb, qui compte 82 protons et 126 neutrons, soit 208 nucléons ! Le noyau pensé comme un mélange homogène de protons et de neutrons ne peut rendre compte de cette texture molle où les 11 ingrédients prennent leurs aises dans un très grand volume.
Aussitôt baptisé "noyau à halo", le lithium 11 a été rejoint par d'autres acolytes du même genre : l'hélium 6 ou le béryllium 11... Comment expliquer leur étendue ? Un modèle théorique a été proposé : le lithium 11 est en fait un lithium 9 entouré de deux neutrons un peu détachés. D'où la dénomination de halo. Pour tester ce modèle, des expériences menées au Ganil ont tenté de casser un noyau de lithium 11 : au sein des débris, deux neutrons ont continué leur course sans être déviés, une indication qu'ils faisaient bien "bande à part" dans le noyau. Mais au rayon des "dissidences nucléaires", les physiciens n'étaient pas au bout de leurs surprises. Car ils ont découvert que certains noyaux semblent en renfermer deux autres, plus petits ! Une véritable hérésie pour les modèles théoriques. Ainsi, le béryllium 12, noyau exotique, peut se décomposer en deux noyaux d'hélium 6... Et que dire de notre carbone ordinaire, le carbone 12, autour duquel s'organise la vie tout entière : dans certaines conditions, il se transforme en trois noyaux d'hélium 4... Faut-il les appeler des noyaux à tiroirs, des noyaux poupées russes ? Sacrée épine dans le pied des théoriciens... qui n'ont pas fini de tourner autour du noyau !
A.K. - SCIENCES ET AVENIR HS > Mai > 2010 |


